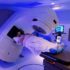
Десять вопросов и десять ответов в онкологии: состояние исследований и прогресс в борьбе против рака
В мире каждый день тысячи человек получают диагноз «рак». Хирургия и профилактика по-прежнему важны сегодня, но, несмотря на здоровый образ жизни, можно заболеть, потому что генетический код нуждается в постоянной поддержке, а с возрастом определенные защитные механизмы могут быть менее сильны.
Кроме того, вероятность того, что хирургическое вмешательство будет решительным, варьируется от случая к случаю. Однако, лекарственные средства развиваются благодаря новым знаниям генетики. На каком этапе находится исследования и что мы ожидаем от будущего? Вот десять ответов на десять вопросов.
Вопросы и ответы отредактированы специалистами Итальянского общества фармакологов и были выпущены 4 февраля — во Всемирный день борьбы против рака (World Cancer Day 2019). На вопросы, которые являются предметом ежедневного обсуждения отвечает Джанни Сава, профессор университета Триеста Италия.
Благодаря новым лекарствам сегодня можно исцелить от рака?
Ответ — да. Очевидно, это зависит от типа рака и особенностей пациента. Природа этого заболевания настолько многогранна, что было бы правильнее говорить во множественном числе об опухолях. Кроме того, индивидуальная компоненты также влияют. У каждого из нас разные гены и, следовательно, мы по-разному реагируем на одну и ту же опухоль и лекарственные средства. Для того, чтобы получить показатель эффективности лечения мы рассуждаем с точки зрения выживания в пять лет, десять лет после установления диагноза, и так далее. А когда невозможно искоренить заболевание, мы пытаемся хронизировать его развитие с помощью лекарств: это означает, что раковые клетки все еще остаются в организме, но у них нет времени на формирование массы, несовместимой с жизнью пациента.
2. Почему трудно полностью уничтожить опухоль?
Потому, что раковые клетки очень похожи на здоровые, и поэтому методы лечения не позволяют точно отличить больные клетки от здоровых. В этом случае мы не всегда можем лечить пациента высокими дозами лекарств, хотя и эффективными, потому что существует риск убить и нормальные клетки, вызывая тяжелые побочные эффекты у пациента. Но вот уже двадцать лет селективность противоопухолевых препаратов в отношении больных клеток значительно возросла. Задача по-прежнему состоит в том, чтобы определить конкретные цели, которые обнаруживаются только на раковых клетках, чтобы поразить их, не убивая здоровые ткани, ставя под угрозу здоровье и физическую работоспособность пациента.
3. Эффективна ли противоопухолевая химиотерапия?
Ответ — да. Проблема старой химиотерапии заключалась в низкой селективности, способности атаковать даже здоровые клетки, вызывая побочные эффекты. Классическая химиотерапия, основанная на использовании цитотоксических веществ, то есть способных к захоронению опухолевых клеток, нарушая их механизмы роста, все еще играет важную роль. Мы научились назначать лекарства целенаправленно, с меньшим количеством побочных эффектов: химиотерапия по-прежнему очень важна при раке крови у детей, и ее часто используют в сочетании с самыми современными противораковыми, биологическими и биотехнологическими препаратами, что приводит к значительному увеличению продолжительности жизни даже в случае особенно агрессивных опухолей.
4. Эффективна ли противоопухолевая радиотерапия?
Определенно, ответ да. Лучевая терапия используется в борьбе с раком благодаря его способности наносить непоправимый ущерб ДНК раковых клеток, причем, механизм действия аналогичен многим препаратам классической химиотерапии. Лучевая терапия, однако, имеет то преимущество, что она более точно нацелена на область, пораженную новообразованием, благодаря оборудованию, способному водить пучок излучения под разными углами. Таким образом, здоровая ткань подвергается воздействию только при низких дозах облучения, и мы можем сконцентрировать больше лучей на отдельных опухолевых мишенях, которые, таким образом, получают огромные дозы очень точным способом.
5. Существуют ли более точные и менее инвазивные стратегии химиотерапии и лучевой терапии?
В Италии есть много новых, более селективных лекарств. Давайте возьмем несколько примеров. Новые соединения, называемые ингибиторами тирозинкиназы (тирозинкиназы являются структурами-мишенями, которые позволяют раковым клеткам связываться с другими клетками), привели к открытию иматиниба, молекулы, способной контролировать рост опухолей, в которых роль этих структур (тирозинкиназа) жизненно необходима. Существуют также многочисленные варианты тирозинкиназ, каждая из которых обладает специфической способностью нацеливаться на разные генетические варианты. Естественно, есть много других целей, типичных для опухолей: речь всегда идет о нарушении жизнедеятельности больной клетки. Например, ингибиторы протеасома влияют на молекулярную систему, ответственную за обеспечение жизнеспособности клеток (например, Бортезомиб и Карфилзомиб), в то время как ингибиторы mTOR может влиять на функционирование многих метаболических путей (например, Темсиролимус и Эверолимус).
6. Если генетика настолько детерминантна в опухолях, мы не могли бы вылечить их с помощью генной терапии?
Возможность вмешательства на опухолях с помощью генной терапии является одной из задач онкологических исследований. Например, недавно мы говорили о результатах, полученных с помощью терапии, известной как CAR-T, где берутся лимфоциты, клетки иммунной системы пациента, и их ДНК модифицируется, чтобы научить их распознавать и атаковать раковые клетки. Обработанные (сконструированные) лимфоциты реинфузируют у субъекта и оказываются способными распознавать и разрушать опухолевые клетки в кровотоке. Успехи, достигнутые с некоторыми новообразованиями крови, являются многообещающими, и в настоящее время исследования направлены на использование этой генной стратегии также для терапии других опухолей.
7. Можно ли разработать вакцину для «предотвращения» опухолей?
Вакцина работает, повышая чувствительность иммунной системы к нежелательному хозяину, обычно вирусу или бактерии. Оба, как только они проникли в организм, воспринимаются как посторонние элементы, потому что они состоят из молекул, очень отличающихся от молекул клеток, составляющих наше тело. К сожалению, раковые клетки, хотя и «чужеродные», как вирусы и бактерии, химически очень похожи на здоровые клетки. И поэтому стратегия вакцинации усложняется тем, что их трудно различить и выборочно повлиять на них. Еще более усложняет тот факт, что раковые клетки посылают сигналы, которые усыпляют иммунную систему. В настоящее время возможны противоопухолевые прививки против некоторых видов рака, таких как рак шейки матки, вызванных вирусом папилломы. Вакцинация подростков против этого вируса, передаваемого половым путем, основной причины возникновения рака, дает отличные результаты.
8. Вместо вакцины можно было бы непосредственно вводить противоопухолевые антитела?
Одним из важных аспектов, на которых сосредоточились исследователи, было избирательное нацеливание на опухолевые клетки, таким образом избегая того, чтобы противораковое лекарственное средство также воздействовало на здоровые клетки. Цели традиционной химиотерапии распределяются между раковыми клетками и здоровыми клетками, и это неизбежно вызывает побочные эффекты, такие как мукозит, расстройства пищеварения, лимфо-, тромбоцитарная и эритропенизация, выпадение волос и другие эффекты. все еще часто характерно для одного активного ингредиента. Возможным решением этих ограничений является использование антитела в онкологии, сконструированного таким образом, чтобы оно могло распознавать конкретную мишень. В химиотерапии принцип состоит в том, что часто поражаемая цель также присутствует в здоровых клетках, но, как правило, в раковых клетках она встречается чаще и в большей степени участвует в выживании самой клетки.
9. Какие опухоли сегодня можно лечить антителами?
Например, моноклональные антитела позволяют точно распознавать мишень на опухолевой клетке, стратегию, которая уже привела к таким сочетаниям терапии, как гентузумаб-озогамицин для терапии острого миелоидного лейкоза, брентуксимаб-ведотин для рецидивов лимфомы Ходжкина и для крупноклеточных анапластических лимфом, Ado-Trastuzumab-emtansine для HER-2-положительного рака молочной железы, Inotuzumab-ozogamicin для острого и B-клеточного лейкоза и Vadastuximab-talirine для острого миелоидного лейкоза. Другие комбинации находятся в стадии клинической разработки.
10. Какие препараты, на которые исследователи возлагают большие надежды?
Поскольку генетика является ключевой, поскольку она позволяет различать раковые клетки и здоровые клетки, величайшие инновации будут получены в результате достижений в области генетики опухолей. В дополнение к прецизионной медицине, новая граница смотрит на мутации, направлена на разработку нового поколения агностических препаратов, способных нацеливаться на все виды рака, которые имеют одну и ту же генную мутацию, независимо от гистологических характеристик, то есть типа ткани или орган происхождения. Таким образом, скоро сможем лечить много разных видов рака одной и той же молекулой.